Chloraceton
Vzhled
| Chloraceton | |
|---|---|
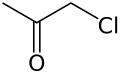 Zjednodušený strukturní vzorec | |
 Strukturní vzorec | |
| Obecné | |
| Systematický název | Chlorpropanon |
| Anglický název | Chloroacetone |
| Německý název | Chloraceton |
| Funkční vzorec | CH3COCH2Cl |
| Sumární vzorec | C3H5ClO |
| Vzhled | bezbarvá kapalina, oxidací mění barvu na zlatohnědou |
| Identifikace | |
| Registrační číslo CAS | 78-95-5 |
| PubChem | 6571 |
| SMILES | ClCC(=O)C |
| InChI | InChI=1/C3H5ClO/c1-3(5)2-4/h2H2,1H3 |
| Vlastnosti | |
| Molární hmotnost | 92,524 g/mol |
| Teplota tání | −44,5 °C |
| Teplota varu | 119 °C |
| Hustota | 1,15 g/cm3 (20 °C/kapalný) |
| Rozpustnost ve vodě | 10 g/100 ml |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Teplota vznícení | 610 °C |
| Meze výbušnosti | 3,4 % |
Některá data mohou pocházet z datové položky. | |
Chloraceton je chemická sloučenina patřící mezi organické sloučeniny, její vzorec je CH3COCH2Cl.
Příprava
[editovat | editovat zdroj]Vzniká přímou chlorací acetonu (zaváděním plynného chloru do acetonu) za kyselé katalýzy.
- CH3-CO-CH3 + Cl2 → Cl-CH2-CO-CH3 + HCl.
Tímto způsobem lze připravit i další halogenderiváty ketonů (např. jodaceton, bromaceton…) Halogenace ketonů probíhá zpravidla velmi snadno, dokonce již ve vodném prostředí.
Může vznikat též reakcí kyseliny chlorné nebo chlornanu (nejlépe vápenatého Ca(ClO)2) a acetonu v kyselém prostředí:
- CH3-CO-CH3 + HClO → Cl-CH2-CO-CH3 + H2O
Vlastnosti
[editovat | editovat zdroj]Je silně dráždivý. Jeho páry způsobují slzení, proto se používá jako bojová slzotvorná látka. Jeho toxicita je za prahem snesitelnosti, tudíž otrava jím je nepravděpodobná.
Odkazy
[editovat | editovat zdroj]Související články
[editovat | editovat zdroj]Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu chloraceton na Wikimedia Commons
Obrázky, zvuky či videa k tématu chloraceton na Wikimedia Commons
Reference
[editovat | editovat zdroj]- ↑ a b Chloroacetone. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)





