다이포스핀

다이포스핀(diphosphines)은 때때로 비스포스판(bisphosphanes)이라고도 불리며, 무기화학 및 유기금속화학에서 두 자리 포스핀 리간드로 가장 흔히 사용되는 유기 인 화합물이다. 이들은 백본으로 연결된 두 개의 포스피노 그룹이 존재함으로써 식별되며, 일반적으로 킬레이트를 형성한다.[1] 다양한 링커와 R-그룹을 가진 다양한 다이포스핀이 합성되었다. 링커와 R-그룹의 변경은 리간드의 전자적 및 입체적 특성을 변화시켜 균일 촉매에서 다른 배위 기하학 및 촉매 거동을 초래할 수 있다.[2]
합성
[편집]
포스파이드 빌딩 블록으로부터
[편집]
많은 널리 사용되는 다이포스핀 리간드는 일반식 Ar2P(CH2)nPAr2를 갖는다. 이 화합물은 X(CH2)nX (X=할로젠)와 MPPh2 (M = 알칼리 금속)의 반응으로 제조될 수 있다.[3]
- Cl(CH2)nCl + 2 NaPPh2 → Ph2P(CH2)nPPh2 + 2 NaCl
다이포스핀 리간드는 또한 다이리튬화된 시약과 클로로포스핀으로부터 제조될 수 있다.[4]
- XLi2 + 2 ClPAr2 → X(PAr2)2 + 2 LiCl (X = 탄화수소 골격)
이 접근법은 클로로다이아이소프로필포스핀과 같은 시약을 사용하여 두 개의 다이알킬포스피노 그룹을 도입하는 데 적합하다.
비대칭 다이포스핀을 제조하는 데 적합한 또 다른 인기 있는 방법은 이차 포스핀을 비닐포스핀에 첨가하는 것을 포함한다.
- Ph2PH + 2 CH2=CHPAr2 → Ph2PCH2-CH2PAr2
(2-리튬페닐)다이페닐포스핀도 비대칭 다이포스핀을 생성하는 데 사용될 수 있다. 리튬화된 시약은 (2-브로모페닐)다이페닐포스핀으로부터 얻을 수 있다.
- Ph2P(C6H4Br) + BuLi → Ph2P(C6H4Li) + BuBr
- Ph2P(C6H4Li) + R2PCli → Ph2P(C6H4PR2) + LiCl
비스(다이클로로포스핀) 전구체로부터
[편집]많은 다이포스핀은 X(PCl2)2 유형의 화합물로부터 제조되며, 여기서 X = (CH2)n 또는 C6H4이다. 주요 시약은 1,2-비스(다이클로로포스피노)에테인 및 1,2-비스(다이클로로포스피노)벤젠이다.

사슬 길이 및 배위 특성
[편집]짧은 사슬 다이포스핀인 dppm은 A-프레임 착물에서 볼 수 있듯이 금속-금속 상호작용을 촉진하는 경향이 있다. 두 개의 포스핀 치환기가 2개에서 4개의 탄소 중심에 의해 연결될 때, 결과적인 리간드는 종종 단일 금속과 함께 킬레이트 고리를 형성한다. 일반적인 다이포스핀 리간드는 dppe이며, 대부분의 금속과 함께 5원자 킬레이트 고리를 형성한다.
tBu2P(CH2)10PtBu2와 같은 특이한 경우를 포함한 일부 다이포스핀은 고리에 최대 72개의 원자를 가진 거대고리 착물을 생성한다.[7]
배위 구면에 포스핀 주개 그룹을 트랜스로 배치하려면 주개 중심을 연결하기 위해 여러 원자가 필요하며, 긴 사슬 다이포스핀은 일반적으로 유연하여 킬레이트를 잘 형성하지 않는다. 이 문제는 길지만 단단한 다이포스핀인 SPANphos에 의해 해결되었다.[8] 다이포스핀의 물림각은 금속 중심의 반응성에 영향을 미친다.[9]
일부 비킬레이트 다이포스핀의 예도 존재한다. 입체 효과로 인해 이들 인 원자는 양성자를 제외하고는 어떤 것과도 반응할 수 없다. [10] 연결 팔의 길이를 조절하여 비킬레이트에서 킬레이트 다이포스핀으로 변경할 수 있다.[11]
대표적인 리간드
[편집]특히 흔한 다이포스핀 리간드는 아래 표에 나와 있다.[12]
| 약어 | 일반명 (약어의 유래) |
구조 | 물림각 |
|---|---|---|---|
| dppm | 1,1-비스(다이페닐포스피노)메테인 | 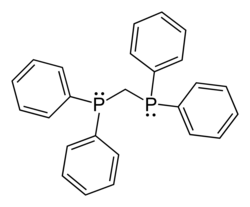
|
73 |
| dmpe | 1,2-비스(다이메틸포스피노)에테인 | 
|
|
| dippe | 1,2-비스(다이아이소프로필포스피노)에테인 | 
|
|
| dppbz | 1,2-비스(다이페닐포스피노)벤젠 | 
|
|
| dppe | 1,2-비스(다이페닐포스피노)에테인 | 
|
86 |
| DIPAMP | 페닐아니실메틸포스핀 유도체 | 
|
|
| dcpe | 비스(다이사이클로헥실포스피노)에테인 | 
|
|
| dppp | 1,3-비스(다이페닐포스피노)프로페인 | 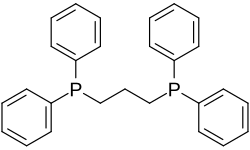
|
91 |
| dppb | 1,4-비스(다이페닐포스피노)뷰테인 | 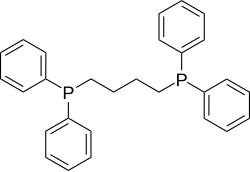
|
94 |
| DIOP | (S,S)-DIOP (O-아이소프로필리덴-2,3-다이하이드록시-1,4-비스(다이페닐포스피노)뷰테인) | 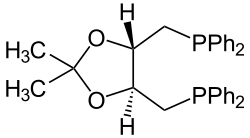
|
|
| 키라포스 | 2,3-비스(다이페닐포스피노)뷰테인 | 
|
|
| BINAP | 2,2'-비스(다이페닐포스피노)-1,1'-바이 naphthyl | 
|
93 |
| Xantphos | 4,5-비스(다이페닐포스피노)-9,9-다이메틸잔텐 | 
|
108 |
| DPEphos | 비스[(2-다이페닐포스피노)페닐] 에터 | 
|
104 |
| SPANphos | 4,4,4',4',6,6'-헥사메틸-2,2'-스피로바이크로만-8,8'-다이일비스(다이페닐포스판) | 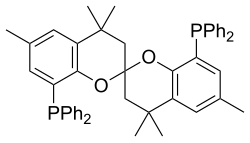
|
|
| SEGPHOS | 4,4'-바이-1,3-벤조다이옥솔-5,5'-다이일비스(다이페닐포스판) | 
|
|
| dppf | 1,1'-비스(다이페닐포스피노)페로센 | 
|
99 |
| Me-DuPhos | 1,2-비스(2,5-다이메틸포스폴라노)벤젠 | 
|
|
| Josiphos | (다이페닐포스피노)페로세닐-에틸다이사이클로헥실포스핀1,5-다이아자-3,7-다이포스파사이클로옥테인 | ![일반적인 조시포스 리간드[3]](https://upload.wikimedia.org/wikipedia/commons/thumb/6/63/Josiphos.png/250px-Josiphos.png)
|
|
| P2N2 | 1,5-다이아자-3,7-다이포스파사이클로옥테인 | 
|
같이 보기
[편집]각주
[편집]- ↑ Hartwig, J. F. Organotransition Metal Chemistry, from Bonding to Catalysis; University Science Books: New York, 2010. ISBN 189138953X
- ↑ Clevenger, Andrew L.; Stolley, Ryan M.; Aderibigbe, Justis; Louie, Janis (2020). 《Trends in the Usage of Bidentate Phosphines as Ligands in Nickel Catalysis》. 《Chemical Reviews》 120. 6124–6196쪽. doi:10.1021/acs.chemrev.9b00682. PMID 32491839.
- ↑ Wilkinson, G.; Gillard, R.; McCleverty, J. Comprehensive Coordination Chemistry: The synthesis, reactions, properties & applications of coordination compounds, vol.2.; Pergamon Press: Oxford, UK, 1987; p. 993. ISBN 0-08-035945-0
- ↑ Gareth J. Rowlands "Planar Chiral Phosphines Derived from [2.2]Paracyclophane" Israel Journal of Chemistry 2012, Volume 52, Issue 1-2, pages 60–75.doi:10.1002/ijch.201100098
- ↑ Burt, Roger J.; Chatt, Joseph; Hussain, Wasif; Leigh, G.Jeffery (1979). 《A convenient synthesis of 1,2-bis(dichlorophosphino)ethane, 1,2-bis(dimethylphosphino)ethane and 1,2-bis(diethylphosphino)ethane》. 《Journal of Organometallic Chemistry》 182. 203–206쪽. doi:10.1016/S0022-328X(00)94383-3.
- ↑ Moloy, Kenneth G.; Petersen, Jeffrey L. (1995). 《N-Pyrrolyl Phosphines: An Unexploited Class of Phosphine Ligands with Exceptional .pi.-Acceptor Character》. 《Journal of the American Chemical Society》 117. 7696–7710쪽. Bibcode:1995JAChS.117.7696M. doi:10.1021/ja00134a014.
- ↑ Cotton, F.A.; Wilkinson, G. Advanced Inorganic Chemistry: A Comprehensive Text, 4th ed.; Wiley-Interscience Publications: New York, NY, 1980; p.246. ISBN 0-471-02775-8
- ↑ Z. Freixa, M. S. Beentjes, G. D. Batema, C. B. Dieleman, G. P. F. v. Strijdonck, J. N. H. Reek, P. C. J. Kamer, J. Fraanje, K. Goubitz and P. W. N. M. Van Leeuwen (2003). 《SPANphos: A C2-Symmetric trans-Coordinating Diphosphane Ligand》. 《앙게반테 케미》 42. 1322–1325쪽. doi:10.1002/anie.200390330. PMID 12645065.
- ↑ Birkholz, M.-N., Freixa, Z., van Leeuwen, P. W. N. M., "Bite angle effects of diphosphines in C-C and C-X bond forming cross coupling reactions", Chem. Soc. Rev. 2009, vol. 38, 1099
- ↑ Zong, J., J. T. Mague, C. M. Kraml, and R. A. Pascal, Jr., A Congested in,in-Diphosphine, Org. Lett. 2013, 15, 2179-2181.
- ↑ Zong, J., J. T. Mague, and R. A. Pascal, Jr., "Encapsulation of non-hydrogen atoms by in, in-bis (triarylelement)-containing cyclophanes." Tetrahedron, 2017, 73, 455-460.
- ↑ http://old.iupac.org/reports/provisional/abstract04/RB-prs310804/TableVII-3.04.pdf [{{{설명}}}]
